அறிவியல் : முதல் பருவம் அலகு 4 : அணு அமைப்பு
மதிப்பீடு
I. சரியான விடையைத் தேர்ந்தெடுக்கவும்
1. பருப்பொருளின் அடிப்படை அலகு __________ ஆகும்.
அ) தனிமம்
ஆ) அணு
இ) மூலக்கூறு
ஈ) எலக்ட்ரான்
விடை : ஆ) அணு
2. அணுக்கருவைச் சுற்றி வரும் அடிப்படை அணுத்துகள் __________ ஆகும்.
அ) அணு
ஆ) நியூட்ரான்
இ) எலக்ட்ரான்
ஈ) புரோட்டான்
விடை : இ) எலக்ட்ரான்
3. __________ நேர் மின்சுமையுடையது.
அ) புரோட்டான்
ஆ) எலக்ட்ரான்
இ) மூலக்கூறு
ஈ) நியூட்ரான்
விடை : அ) புரோட்டான்
4. ஓர் அணுவின் அணு எண் என்பது அதிலுள்ள __________ ஆகும்.
அ) நியூட்ரான்களின் எண்ணிக்கை
ஆ) புரோட்டான்களின் எண்ணிக்கை
இ) புரோட்டான்கள் மற்றும் நியூட்ரான்களின் மொத்த எண்ணிக்கை
ஈ) அணுக்களின் எண்ணிக்கை
விடை : ஆ) புரோட்டான்களின் எண்ணிக்கை
5. நியூக்ளியான்கள் என்பது __________ குறிக்கும்.
அ) புரோட்டான்கள் மற்றும் எலக்ட்ரான்களைக்
ஆ) நியூட்ரான்கள் மற்றும் எலக்ட்ரான்களைக்
இ) புரோட்டான்கள் மற்றும் நியூட்ரான்களைக்
ஈ) நியூட்ரான்கள் மற்றும் பாஸிட்ரான்களைக்
விடை : இ) புரோட்டான்கள் மற்றும் நியூட்ரான்களைக்
II. கோடிட்ட இடங்களை நிரப்புக
1. ஒரு அணுவில் காணப்படும் மிகச்சிறிய துகள் _________
விடை : அணுக்கூறுகள்
2. அணுவின் உட்கருவில் __________ மற்றும் __________ இருக்கும்.
விடை : புரோட்டான்கள், நியூட்ரான்கள்
3. அணுவின் உட்கருவை __________ சுற்றி வரும்
விடை : எலக்ட்ரான்கள்
4. கார்பனின் இணைதிறன் 4 மற்றும் ஹைட்ரஜனின் இணைத்திறன் 1 ஆக உள்ளது எனில், மீத்தேனின் மூலக்கூறு வாய்ப்பாடு __________
விடை : CH4
5. மெக்னீசியம் அணுவின் வெளிவட்டப் பாதையானது இரண்டு எலக்ட்ரான்களைக் கொண்டிருக்கிறது எனில் மெக்னீசியம் அணுவின் இணைதிறன் __________.
விடை : இரண்டு
III. பொருத்துக
1. இணைதிறன் – அ. Fe
2. மின்சுமையற்ற துகள் – ஆ. புரோட்டான்
3. இரும்பு – இ. வெளிவட்டப்பாதையில் காணப்படும் எலெக்ட்ரான்
4. ஹைட்ரஜன் – ஈ. நியூட்ரான்
5. நேரமின்சுமை கொண்ட துகள் – உ. ஒற்றை இணைதிறன்
விடைகள் :
1. இணைதிறன் – இ. வெளிவட்டப்பாதையில் காணப்படும் எலெக்ட்ரான்
2. மின்சுமையற்ற துகள் – ஈ. நியூட்ரான்
3. இரும்பு – அ. Fe
4. ஹைட்ரஜன் – உ. ஒற்றை இணைதிறன்
5. நேரமின்சுமை கொண்ட துகள் – ஆ. புரோட்டான்
IV. சரியா அல்லது தவறா எனக் கூறுக. தவறான கூற்றைத் திருத்தி எழுதுக
1. ஒரு தனிமத்தின் அடிப்படை அலகு மூலக்கூறு ஆகும்.
விடை : தவறு. ஒரு தனிமத்தின் அடிப்படை அலகு அணு ஆகும்
2. எலெக்ட்ரான்கள் நேர்மின்சுமை கொண்டவை
விடை : தவறு. எலெக்ட்ரான்கள் எதிர்மின்சுமை கொண்டவை
3. ஓர் அணு மின்சுமையற்ற நடுநிலைத் தன்மையை கொண்டது
விடை : சரி
4. அணுவின் உட்கருவைச் சுற்றி புரோட்டான்கள் காணப்படுகின்றன.
விடை : தவறு. அணுவின் உட்கருவைச் சுற்றி எலக்ட்ரான்கள் காணப்படுகின்றன.
V. ஒப்புமை தருக
1. சூரியன் : உட்கரு :: கோள்கள் : __________.
விடை : எலக்ட்ரான்கள்
2. அணு எண் : __________ :: நிறை எண் : புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கை.
விடை : புரோட்டான்கள் (அ) எலக்ட்ரான்களின் எண்ணிக்கை
3. K : பொட்டாசியம் :: C : __________.
விடை : கார்பன்
VI. கீழ்க்காணும் கூற்றுக்களை ஆராய்ந்து, சரியான ஒன்றைத் தேர்வு செய்க
அ) கூற்று மற்றும் காரணம் இரண்டும் சரி. காரணம் கூற்றிற்கான சரியான விளக்கம்
ஆ) கூற்று மற்றும் காரணம் இரண்டும் சரி. ஆனால் காரணம் கூற்றிற்கான சரியான விளக்கமல்ல
இ) கூற்று சரி. ஆனால், காரணம் தவறு
ஈ) கூற்று தவறு. ஆனால், காரணம் சரி
1. கூற்று : ஓர் அணு மின்சுமையற்றது, நடுநிலையானது
காரணம் : அணுக்கள் சம எண்ணிக்கையிலான புரோட்டான்களையும் எலக்ட்ரான்களையும் கொண்டவை.
விடை : அ) கூற்று மற்றும் காரணம் இரண்டும் சரி. காரணம் கூற்றிற்கான சரியான விளக்கம்
2. கூற்று : ஓர் அணுவின் நிறை என்பது அதன் உட்கருவின் நிறையாகும்.
காரணம் : உட்கரு மையத்தில் அமைந்துள்ளது.
விடை : ஆ) கூற்று மற்றும் காரணம் இரண்டும் சரி. ஆனால் காரணம் கூற்றிற்கான சரியான விளக்கமல்ல
சரியான விளக்கம் : அணுவின் நிறை என்பது புரோட்டான்கள் மற்றும் நியூட்ரான்களின் கூடுதல்.
3. கூற்று : புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கை அணு
எண்ணாகும்.
காரணம் : புரோட்டான்கள் மற்றும் நியூட்ரான்களின் மொத்த எண்ணிக்கை நிறை எண்ணாகும்.
விடை : ஈ) கூற்று தவறு. ஆனால், காரணம் சரி
சரியான விளக்கம் : புரோட்டான்கள் அல்லது எலக்ட்ரான்களின் எண்ணிக்கை அணு எண்ணாகும்.
VII. மிகச் சுருக்கமாக விடையளி
1. அணு – வரையறு.
பருப்பொருள்களை உருவாக்கும் மிகச் சிறிய துகள்களே அணுக்கள் எனப்படும்.
2. அணுவின் அடிப்படைத் துகள்களைக் குறிப்பிடவும்.
புரோட்டான்கள், நியூட்ரான்கள் மற்றும் எலக்ட்ரான்கள்
3. அணு எண் என்றால் என்ன?
ஓர் அணுவில் உள்ள புரோட்டான்கள் அல்லது எலக்ட்ரான்களின் எண்ணிக்கையே அணு எண் எனப்படும்.
4. புரோட்டானின் பண்புகள் யாவை?
• புரோட்டான் அணுவின் மிகச்சிறிய அணுக்கூறு ஆகும்.
• புரோட்டான்கள் அணுக்கருவினுள் அமைந்துள்ளன.
• புரோட்டான்கள் நேர்மின்னூட்டம் பெற்ற துகள்கள் ஆகும்.
• புரோட்டான்கள் நேர்மின்னூட்டத்தின் மதிப்பு எலக்ட்ரான் பெற்றுள்ள எதிர் மின்னூட்டத்தின் மதிப்பிற்குச் சமமாகும்.
5. நியூட்ரான்கள் ஏன் மின்சுமையற்ற துகள்கள் என அழைக்கப்படுகின்றன?
• நியூட்ரான்கள் எவ்வித மின்சுமையும் கொண்டிருக்கவில்லை.
• எனவே நியூட்ரான்கள் மின்சுமையற்ற துகள்கள் என அழைக்கப்படுகின்றன.
VIII. சுருக்கமாக விடையளி
1. ஐசோடோப்புகள், ஐசோபார்கள் – வேறுபடுத்தவும்.

ஐசோடோப்புகள்
1. ஒரே அணு எண்ணையும், வெவ்வேறு நிறை எண்களையும் பெற்றுள்ள ஒரே தனிமத்தின் அணுக்கள்.
2. ஒரே புரோட்டான்கள் மற்றும் எலக்ட்ரான்கள் எண்ணிக்கையும் வெவ்வேறு நியூட்ரான்கள் எண்ணிக்கையும் பெற்றுள்ளன.
3. எ.கா. 1H1, 1H2, 1H3
ஐசோபார்கள்
1. ஒரே நிறை எண்ணையும், வெவ்வேறு அணு எண்களையும் கொண்ட வெவ்வேறு தனிமத்தின் அணுக்கள்.
2. வெவ்வேறு புரோட்டான்கள், எலக்ட்ரான்கள் மற்றும் நியூட்ரான்கள் எண்ணிக்கையைப் பெற்றுள்ளன.
3. எ.கா. 18Ar40, 20Ca40
2. ஐசோடோப்புகள் என்றால் என்ன? ஓர் உதாரணம் தருக.
• ஒரே தனிமத்தின் அணுக்கள் வெவ்வேறு எண்ணிக்கையுள்ள நியூட்ரான்களை பெற்றிருக்கலாம்.
• அத்தகைய அணுக்கள் ஒரே அணு எண்ணையும் வெவ்வேறு நிறை எண்களையும் பெற்றுள்ளன. அவை ஐசோடோப்புகள் என அழைக்கப்படுகின்றன.
• உதாரணம்: புரோட்டியம் (1H1), டியூட்ரியம் (1H2), டிரிட்டியம் (1H3)
3. நிறை எண் மற்றும் அணு எண் வேறுபடுத்துக.
அணு எண்
புரோட்டான்கள், அல்லது எலக்ட்ரான்களின் எண்ணிக்கையை
நிறை எண்
புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கையின் கூடுதல்
4. ஒரு தனிமத்தின் அணு எண் 9 மற்றும் அத்தனிமம் 10 நியூட்ரான்களை கொண்டுள்ளது எனில், தனிம ஆவர்த்தன அட்டவணையினைக் கொண்டு அது எத்தனிமம் எனக் கண்டறிக. அதன் நிறை எண் யாது?
தனிமம் ஃப்ளூரின் ஆகும். 9F19
நிறை எண் A = புரோட்டான் எண்ணிக்கை + நியூட்ரான் எண்ணிக்கை
= அணு எண் + நியூட்ரான் எண்ணிக்கை
= 9 + 10 = 19
IX. விரிவாக விடையளி
1. அணு அமைப்பின் படம் வரைந்து அதன் அடிப்படைத் துகள்களின் நிலையினை விளக்குக
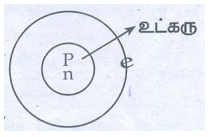
• அணு கோள வடிவமானது.
• நடுவில் உட்கரு அமைந்துள்ளது.
• உட்கருவில் புரோட்டான்கள் மற்றும் நியூட்ரான்கள் உள்ளன.
• எலக்ட்ரான்கள் உட்கருவை வட்டப்பாதையில் சுற்றி வருகின்றன.
2. ஒரு தனிமத்தின் அணு எண் மற்றும் நிறை எண் முறையே 26 மற்றும் 56. அந்த அணுவில் உள்ள எலக்ட்ரான்கள், புரோட்டான்கள் மற்றும் நியூட்ரான்களின் எண்ணிக்கையைக் கணக்கிடுக. அதன் அணு அமைப்பினை வரையவும்.
அணு எண் (Z) = புரோட்டான்களின் எண்ணிக்கை = எலக்ட்ரான்களின் எண்ணிக்கை = 26
நிறை எண் (A) = புரோட்டான்களின் எண்ணிக்கை (Z) + நியூட்ரான்களின் எண்ணிக்கை (N)
A = Z + N
N = A – Z
= 56 – 26 = 30
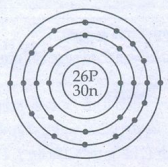
எலக்ட்ரான் அமைப்பு : 2, 8, 14, 2
3. நியூக்ளியான்கள் என்றால் என்ன? அவை ஏன் அவ்வாறு அழைக்கப்படுகின்றன? நியூக்ளியான்களின் பண்புகளை எழுதவும்.
• புரோட்டான்கள் மற்றும் நியூட்ரான்கள் ஆகியன நியூக்ளியான்கள் ஆகும்.
• அணுவின் உட்கருவினுள் இவை காணப்படுவதால் நியூக்ளியான்கள் என அழைக்கப்படுகின்றன
• புரோட்டான்கள் நேர்மின்னூட்டம் பெற்ற துகள்கள் ஆகும்.
• நியூட்ரான்கள் எவ்வித மின்சுமையும் பெற்றிருக்கவில்லை.
• புரோட்டான் மற்றும் நியூட்ரான் ஆகியன ஒத்த நிறையை பெற்றுள்ளன.
4. இணைதிறனை வரையறு. அணு எண் 8 கொண்ட ஒரு தனிமத்தின் இணைதிறன் மதிப்பு என்ன? அத்தனிமம் ஹைட்ரஜனுடன் இணைந்து உருவாக்கும் சேர்மம் யாது?
• ஓர் அணு பிற அணுவுடன் இணையக்கூடிய திறனிற்கு இணை திறன் என்று பெயர்.
• ஓர் அணுவின் இணைதிறன் அது எத்தனை ஹைட்ரஜன் அணுக்களை பிணைத்து வைத்திருக்க இயலும் என்பதனை கொண்டு அளவிடப்படுகிறது.
• அணு எண் 8 கொண்ட தனிமம் ஆக்சிஜன் ஆகும்.
• ஆக்சிஜனின் இணைதிறன் இரண்டு.
• ஒரு ஆக்சிஜன் அணு இரண்டு ஹைட்ரஜன் அணுக்களுடன் இணைந்து ஒரு மூலக்கூறு நீரினை உருவாக்குகிறது.
• நீர் மூலக்கூறின் வாய்பாடு H2O
X. உயர் சிந்தனைத் திறன்கள் அடிப்படையிலான வினாக்கள்
1. ஒரு தனிமத்தின் அணுவில் எலக்ட்ரான் இல்லை எனில் அந்த அணுவிற்கு நிறை உண்டா இல்லையா? ஒரு அணு எலக்ட்ரான் இன்றி இருக்குமா? அவ்வாறு இருந்தால், எடுத்துக்காட்டு தருக.
• ஒரு அணு எலக்ட்ரான் இன்றி இருக்காது.
• ஒரு அணு நடுநிலைத் தன்மையுடன் விளங்க சம எண்ணிக்கையில் புரோட்டான்கள் மற்றும் எலக்ட்ரான்கள் பெற்றிருக்க வேண்டும்.
• எலக்ட்ரான் இல்லாத அணு நேர்மின் அயனியாக இருக்கும்.
• நேர்மின் அயனியில் புரோட்டான் மற்றும் நியூட்ரான்கள் உள்ளதால் அதற்கு நிறை உண்டு.
• எ.கா. H+ அயனியில் ஒரு புரோட்டான் மட்டுமே உள்ளது. நியூட்ரான்கள் இல்லை . எனவே H+ அயனியின் நிறை புரோட்டானின் நிறைக்கு சமம்.
2. சாதாரண உப்பு என்பது யாது? அதிலுள்ள தனிமங்கள் யாவை? சாதாரண உப்பின் மூலக்கூறு வாய்ப்பாட்டினை எழுதுக. அத்தனிமங்களின் அணு எண் மற்றும் நிறை எண் மதிப்பு என்ன? அந்த சேர்மத்திலுள்ள அயனிகளை எழுதவும்.
சாதாரண உப்பு
தனிமங்கள்
மூலக்கூறு வாய்பாடு
அணு எண்
நிறை எண்
அயனிகள்
சோடியத்தின் குளோரைடு
சோடியம் – 11, குளோரின் – 17
சோடியம் – 23, குளோரின் – 35.5
சோடியம் அயனி Na+, குளோரைடு அயனி CI–
XI. செயல்திட்டம் (மாணவர்களுக்கானது)
1. அணுக்கள் எவ்வாறு இருக்கும் என்பதை அறிய மாணவர்களை ஒரு மாதிரியினை உருவாக்கச் செய்யலாம். எலக்ட்ரான் வட்டங்களை உருவாக்க குழாயைச் சுத்தம் செய்யும் மெல்லிய உலோகக் கம்பிகளையும், புரோட்டான்களையும், நியூட்ரான்களையும் குறிப்பிட வெவ்வேறு நிறங்களில் உள்ள பந்துகளையும் எலக்ட்ரான்களைக் குறிப்பிட மணிகளையும் கொடுக்கலாம். மாணவர்கள் அப்பொருள்களைக் கொண்டு அணு மாதிரியை உருவாக்கி வகுப்பறையின் சுவர்களில் தொங்கவிடும் போது மகிழ்ச்சியடைவர்.
மாணவர் செயல்பாடு
ஒரு அணுவானது மனித முடியின் தடிமனைக் காட்டிலும் ஆயிரம் மடங்கு சிறியது. அதன் சராசரி விட்டம் 0.000000001மீ. அல்லது 1× 10-9மீ. ஒரு அணுவின் அளவைப் புரிந்துகொள்வதற்கு, நமக்குத் தெரிந்த சில பொருள்களாகிய பென்சில், இரத்த வெள்ளை அணு, வைரஸ் மற்றும் தூசுகளின் அளவு எவ்வளவு என்று நாம் காண்போம்
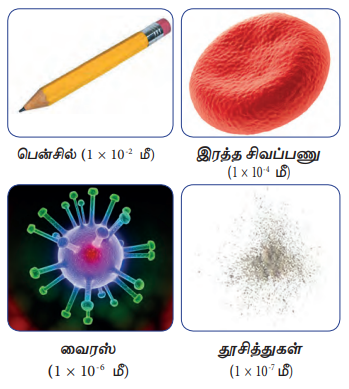
ஒரு அணு எவ்வளவு சிறியது என்பதை உங்களால் இப்பொழுது கற்பனை செய்து பார்க்க முடியும்.
அணுவின் அமைப்பினைப் பற்றி அநேக அறிவியலாளர்கள் ஆய்வுகளை மேற்கொண்டு தங்கள் கொள்கைகளை வெளியிட்டுள்ளனர். டால்டன், தாம்ஸன், ரூதர்போர்டு ஆகியோர் கூறிய கொள்கைகள் இங்கு கொடுக்கப்பட்டுள்ளன.
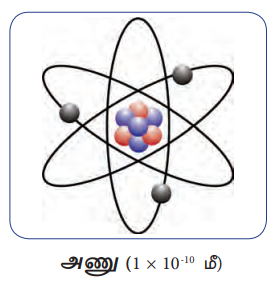
செயல்பாடு 1
நமக்குத் தெரிந்த சில பொருள்கள் மற்றும் அவற்றின் துகள்களின் படங்கள் கீழே கொடுக்கப்பட்டுள்ளன.
பொருள்களின் பெயர்களையும் அவை எத்துகள்களால் உருவானவை என்பதனையும் எழுதுக.

1. சுத்தியல் (இரும்பு )
2. வளையல் (தங்கம் )
3. குழாய் (நிக்கல் )
4. கிண்ணம் (தாமிரம் )
அணுவின் பகுதிப்பொருள்கள் கண்டறியப்பட்ட காலம்
செயல்பாடு 2
கீழ்க்காணும் வரைபடத்தை உற்று நோக்கி பின்வரும் வினாக்களுக்கு விடையளிக்கவும்.
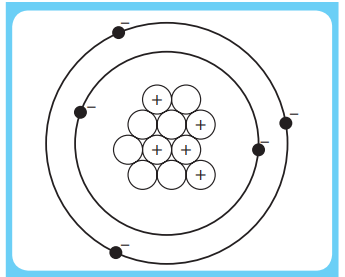
1. புரோட்டான் நேர்மின் சுமை கொண்ட துகளாகும்.
2. எலக்ரான் மின்சுமை அற்றது.
3. எலக்ரான் எதிர்மின்சுமை கொண்ட துகளாகும்.
செயல்பாடு 3

மேலே கொடுக்கப்பட்டுள்ள அட்டவணையினை உற்றுநோக்கி பின்வரும் வினாக்களுக்கு விடையளிக்கவும்.
1. நான் சுவாசித்தலுக்குப் பயன்படுகிறேன். நான் இல்லாமல் உங்களால் உயிர் வாழ முடியாது. எனது பெயரையும், குறியீட்டையும் எழுதுக. ஆக்சிஜன், O.
2. இது பலூன்களை நிரப்பப் பயன்படுகிறது. இது ஒரு வாயுவாகும். இதனை அடையாளம் காண்க. இதன் நிறை எண் என்ன?ஹட்ரஜன். (A=l).
3. வாழைப்பழத்தில் உள்ள தனிமத்தின் பெயரைக் குறிப்பிடுக. அதன் அணு எண் யாது? பொட்டாசியம் (Z = 19)
4. நான் பட்டாசுகளில் காணப்படுகிறேன். நான் எத்தனை புரோட்டான்களைக் கொண்டுள்ளேன்? சல்பர் (p = 16)
5. நான் உயர்ந்த மதிப்புமிக்க தனிமம். நான் யாரென்று கண்டுபிடி. என்னுடைய நிறை எண்ணைக் கூற முடியுமா?
கார்பன் (A= 12)
